Las baterías alcalinas que utilizamos hoy hicieron su debut en 1959. A mediados de la década de 1980, habían superado a las baterías de zinc-carbono como las baterías químicas más populares. Desde su introducción se han consumido miles de millones [probablemente billones] de unidades en todas partes del mundo. Ya en 2009, se estimaba que había 50 mil millones de unidades de pilas alcalinas en circulación, lo que representa un promedio de entre 7 y 8 unidades por individuo cada año.

Hoy en día, el mercado de las pilas alcalinas es una industria multimillonaria que se prevé que seguirá creciendo en el futuro. Este éxito, incluso frente a la competencia de otras químicas de baterías, se debe a algunas propiedades distintas de la química alcalina.
¿Qué es una batería alcalina?
Aunque varias químicas de baterías están diseñadas para funcionar con electrolitos alcalinos , las baterías alcalinas generalmente se refieren a celdas primarias alcalinas de dióxido de zinc y manganeso. En una batería alcalina, el electrodo o cátodo positivo contiene óxido de manganeso (IV), mientras que el electrodo o ánodo negativo contiene zinc.
Las pilas alcalinas iniciales se diseñaron como pilas primarias destinadas a desecharse después de un solo uso. Sin embargo, los avances tecnológicos han llevado al desarrollo de productos químicos alcalinos recargables.
Electroquímica de pilas alcalinas
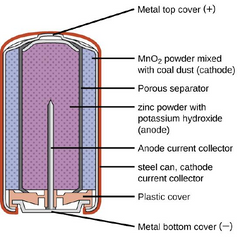
Una batería alcalina produce energía mediante un par de reacciones químicas en sus electrodos positivo y negativo. En el cátodo, el óxido de manganeso (IV) se transforma en óxido de manganeso (III) e iones hidroxilo. Estos iones hidroxilo luego reaccionan con el zinc en el ánodo para liberar electrones generadores de energía.
Aquí hay una ecuación simple para una reacción de celda alcalina:
Zn + 2MnO 2 + H 2 O → ZnO +2MnOOH
En la reacción anterior, se puede ver que se agota el H 2 O (agua). Posteriormente, el cátodo de MnO 2 crea iones hidroxilo (OH-) como se muestra en la siguiente reacción:
2MnO 2 + 2H 2 O+ 2 e → 2MnOOH + 2OH-
Además, el ánodo consume simultáneamente iones hidroxilo mientras crea agua:
Zn + 2OH- →ZnO +H 2 O + 2e
Finalmente, los electrones resultantes (e) de la reacción producen la energía utilizada para diferentes tipos de aparatos o aparatos.
Tamaños de pilas alcalinas
Los tamaños de pilas alcalinas más comunes incluyen:
- Células AAAA
- células AAA
- células AA
- células D
- células C
- N células
- celdas de 9V
- Pilas de botón
Algunas aplicaciones comunes de baterías alcalinas
- Linternas🔦
- Relojes⏰
- Termómetros electrónicos
- Controladores de juego🕹
- Cámaras📷
- Voltímetros digitales
- Controles remotos
- Radios portátiles📻
- Cerraduras de las puertas
- Punteros laser
- juguetes🧸
- Escáneres móviles
- cepillos de dientes electricos
- Transmisores portátiles
- Cepillos de dientes eléctricos, etc.
Factores detrás de la popularidad de las pilas alcalinas
Como se señaló anteriormente, la batería alcalina es ahora la batería más popular después de superar la química de zinc-carbono hace muchos años. Estas son algunas de las razones por las que todavía existe un enorme mercado para las baterías alcalinas, incluso con la aparición de productos químicos más nuevos como NiCD, NiMH y de iones de litio.
☘Alta densidad de energía
Los usuarios que deseen una mayor longevidad encontrarán muy útiles las pilas alcalinas. Esto se debe a que las pilas alcalinas tienen la mayor densidad de energía en comparación con otras sustancias químicas. Por ejemplo, tienen el doble [o más] de densidad energética que las baterías NIMH y de zinc-carbono.
☘Rentable
Las pilas alcalinas suelen ser las más asequibles que encontrará en el mercado. Esto se puede atribuir a unos costes de producción más bajos y a unos componentes químicos comparativamente más baratos.
☘Temperaturas más bajas
Con las pilas alcalinas, no se producirán incidentes de daños en el dispositivo o rendimiento subóptimo debido al sobrecalentamiento. ¿Razón? Las sustancias químicas alcalinas generan menos calor mientras están en funcionamiento.
☘Mayor vida útil
La vida útil es el tiempo que una batería alcalina desechable retendrá su carga sin usar o, en el caso de baterías recargables, cuánto tiempo permanecerá sin usar [sin deterioro significativo] antes de que sea necesario cargarla. La vida útil de una batería puede verse influenciada por ciertos factores, como el diseño, la composición química, la temperatura de almacenamiento y la humedad de la batería.
Las pilas alcalinas no recargables tienen una vida útil de hasta 10 años, una de las más altas de la industria.
☘Mejoras de diseño
La necesidad de una mayor comodidad ha llevado recientemente a mejoras en las técnicas de empaquetado de baterías. Anteriormente, las pilas alcalinas se diseñaban con complejos sistemas de sellado que incluían carcasas exteriores de acero grueso y tapas de extremo. Con el tiempo, estos han ido dando paso gradualmente a nuevos envases únicos, más delgados y sellos más eficientes. Esto se ha traducido en espacio adicional para los componentes de la batería y, por tanto, en una mayor capacidad de rendimiento.
☘Adecuado para macetas.
Debido a que no se caracterizan por cambios de temperatura interna y no son propensas a la formación de gases cuando están en uso activo, las baterías alcalinas son muy adecuadas para encapsular. El encapsulado es un proceso mediante el cual un recinto se llena con un compuesto químico para aumentar su capacidad de resistir golpes y vibraciones y al mismo tiempo proteger cosas como solventes, corrosión y humedad.
☘Disponible en diferentes tamaños.
Como se vio arriba, las baterías alcalinas están diseñadas en diferentes tamaños. Esto los hace cómodos para moverse y fáciles de usar en diferentes tipos de dispositivos domésticos, de oficina y de fábrica.
☘Se puede conectar en serie
Es posible conectar una serie de baterías alcalinas para generar matrices de mayor voltaje. También se pueden organizar en diferentes configuraciones para servir a una amplia gama de propósitos.
☘Más fácil de eliminar/ambientalmente más seguro
Los principales componentes químicos de las pilas alcalinas son el zinc, el manganeso y el acero, todos los cuales son menos tóxicos y, por tanto, no constituyen ninguna amenaza importante ni para la salud humana ni para el medio ambiente. Además, la eliminación del mercurio de la electroquímica de las baterías desde la década de 1990 ha hecho posible deshacerse de las baterías alcalinas gastadas como cualquier otro residuo doméstico en la mayoría de las jurisdicciones.
☘Resistente a fugas
Algunos suelen asociar las pilas alcalinas con roturas y fugas. Pero este no es el caso si opta por pilas alcalinas de calidad de un fabricante de renombre, sobre todo porque hay varios productos en el mercado que no son tan eficientes como otros.
Entonces, ¿qué batería alcalina es mejor para usar?
Con tantas marcas de baterías alcalinas competidoras, a los consumidores definitivamente no les resultará fácil tomar una decisión. Sin embargo, un excelente producto de batería alcalina en el que puede confiar es la EBL cuando se trata de protección antifugas, seguridad, vida útil máxima, longevidad y otras cualidades deseadas en una batería alcalina .
Las baterías alcalinas EBL de alto rendimiento pero muy asequibles se han fabricado con materias primas de primera calidad y tecnología de celdas de alta densidad que brindarán a sus dispositivos suficiente energía y durarán más, lo que permitirá que sus diversos dispositivos funcionen de manera óptima y le permitan ahorrar dinero. Si desea obtener el mejor servicio de una batería alcalina, ¡EBL debería ser su elección! Visite nuestro sitio web hoy para obtener más información.





Dejar un comentario
Todos los comentarios se revisan antes de su publicación.
Este sitio está protegido por hCaptcha y se aplican la Política de privacidad de hCaptcha y los Términos del servicio.